El calorímetro de laboratorio es un instrumento que se utiliza para medir temperaturas, más específicamente, mide el calor que reciben los cuerpos y así determinar el calor específico de estos. También mide la energía que liberan los objetos en forma de calor.
Características
El calorímetro más común, consiste en un envase sellado y aislado, en el cual se coloca agua; un agitador y un termómetro.
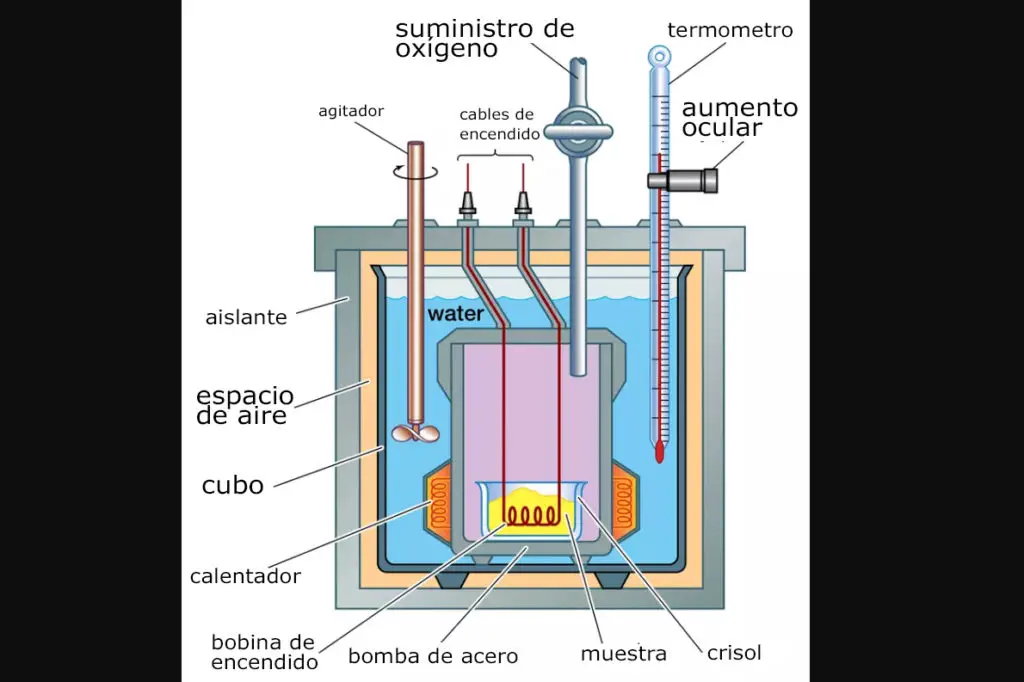
¿Cómo funciona?
La mayoría de estos instrumentos aplican el principio de la carga dual, en esta, una absorbe y la otra mantiene una temperatura de referencia, así el sensor identifica el cambio de la temperatura comparando una con la otra.
Fórmula
Al realizarse el proceso con una presión que es constante, la capacidad calorífica se mide a una presión constante, por ello se utiliza el símbolo Cp.
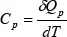
En cambio, si el volumen se mantiene constante, entonces se define la capacidad calorífica con un volumen constante.
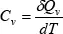
Qp y Qv representan la cantidad de calor que se intercambian con presión y volumen constante.
Microcalorímetro
El microcalorímetro es un tipo de calorímetro que se utiliza más frecuentemente que los demás. Es un instrumento que registra la eficiencia efectiva de un montaje bolo métrico. Su invención está relacionada con la calibración de metal wire bolometers.
Calorímetro adiabático
En este tipo de calorímetro, la temperatura en el escudo se encuentra muy cerca de la temperatura de la celda, esto evita la transferencia de calor.
Cuando se utiliza el término adiabático, nos referimos a una aproximación a una medida ideal, ya que se tiene un control de las variables para realizar el modelo.

